У Китаї штучний інтелект у медицині дедалі частіше працює як «другі очі» для лікарів. Найпомітніший приклад — спроба ловити рак підшлункової залози на рутинних КТ, де навіть досвідчений радіолог може не побачити ранні, ледь помітні зміни у щоденному потоці знімків.
Рак підшлункової залози — одна з найсмертельніших онкологій: загальна 5-річна виживаність за сучасними оцінками становить близько 10–13%. Проблема не лише в лікуванні, а в часі: симптоми часто з’являються, коли пухлина вже неоперабельна, і шанс різко падає.
Скринінг цієї хвороби складний, бо «золоті» тести на кшталт контрастної КТ або інших методів дають більше опромінення і не підходять для масового застосування. Натомість КТ без контрасту дешевші та поширені, але картинка менш контрастна, і ураження легко зливається з фоном.
На цьому тлі з’явився алгоритм PANDA (pancreatic cancer detection with artificial intelligence). Його навчили шукати ознаки пухлин саме на КТ без контрасту, тобто на тому типі знімків, який у багатьох клініках роблять «за замовчуванням» для інших задач — від огляду грудної клітки до контролю живота.
Пілотний проєкт запустили в Affiliated People’s Hospital of Ningbo University як клінічне випробування в листопаді 2024 року. Важлива деталь: система не змушує пацієнта проходити додаткові обстеження на старті, а аналізує вже зроблені знімки й лише тоді створює запит на уточнення.
 Кіоски самообслуговування у Народній лікарні Університету Нінбо. Лікарня в Нінбо, Китай, тестує інструмент на базі штучного інтелекту для виявлення раку підшлункової залози — Андреа Верделлі
Кіоски самообслуговування у Народній лікарні Університету Нінбо. Лікарня в Нінбо, Китай, тестує інструмент на базі штучного інтелекту для виявлення раку підшлункової залози — Андреа Верделлі
За даними лікарів Нінбо, PANDA вже переглянула понад 180 тисяч КТ грудної клітки або черевної порожнини. Вона допомогла знайти близько двох десятків випадків раку підшлункової, причому 14 — на ранній стадії. Частину знімків раніше не сприймали як тривожні, поки їх не підсвітив ШІ.
Історія Цю Сицзюня показує логіку «опортуністичного скринінгу». Чоловік прийшов на стандартний контроль діабету, зробив рутинну КТ, а за кілька днів отримав дзвінок від профільного хірурга. Пухлину знайшли до симптомів і видалили, що різко змінило прогноз для пацієнта.
Технологічно Китай робить ставку на масштаб: у багатьох містах люди проходять КТ без контрасту в рамках щорічних чек-апів, тож дані вже є. Якщо до потоку під’єднати нейромережу, то можна підняти частку «випадково» виявлених ранніх стадій без тотального розгортання дорогих програм скринінгу.
Розробку пов’язують із Alibaba DAMO Academy та пов’язаними дослідниками. У статті Nature Medicine (2023) описано модель, що з неконтрастних КТ визначає не лише панкреатичну протокову аденокарциному, а й низку інших уражень підшлункової — від нейроендокринних пухлин до хронічного панкреатиту.
Критичне питання було простим: як навчити модель на «бідних» зображеннях, якщо найчіткіші ураження видно на контрастній КТ? Рішення: радіолог вручну промаркував ураження на контрастних знімках тисяч пацієнтів, а мітки алгоритмічно перенесли на їхні КТ без контрасту.
Після такого навчання автори повідомляли, що на великій вибірці неконтрастних КТ система виявляла більшість пацієнтів з ураженнями. Але навіть сильні метрики в статті не гарантують успіху в потоці реальної лікарні, де протоколи й якість знімків різняться.
У Нінбо PANDA працює як фільтр: вона видає «ризиковий» сигнал, а далі команда переглядає знімок, звіряє клінічні симптоми й вирішує, чи потрібні уточнювальні тести. Це принципова межа: ШІ не ставить діагноз, а змінює чергу пацієнтів і швидкість їх потрапляння до спеціаліста.
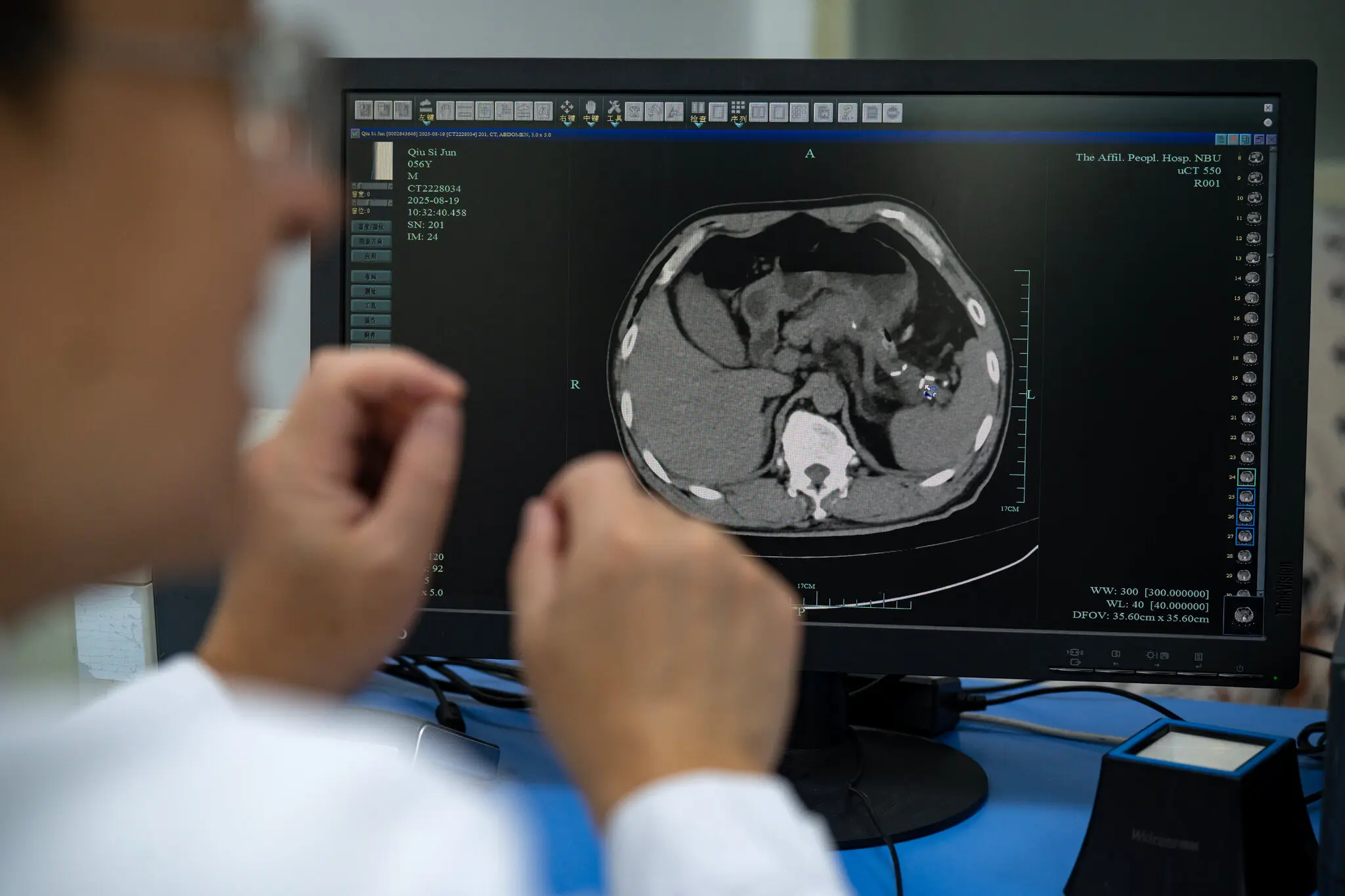 Вивчення одного зі сканів пана Цю. Прилад шукає рак підшлункової залози на безконтрастних комп'ютерних томографіях, які не показують аномалії так чітко, як сканування з контрастним барвником — Андреа Верделлі
Вивчення одного зі сканів пана Цю. Прилад шукає рак підшлункової залози на безконтрастних комп'ютерних томографіях, які не показують аномалії так чітко, як сканування з контрастним барвником — Андреа Верделлі
Найбільший системний ризик — хибнопозитивні результати. Помилка запускає страх «підозри на рак», додаткові обстеження й інколи інвазивні процедури. Для рідкісних хвороб це боляче: малий відсоток хибних тривог перетворюється на сотні зайвих викликів вчасно.
У пілоті система видала близько 1 400 сповіщень, але лише приблизно 300 випадків лікарі віднесли до тих, що реально потребують фоллоу-апу. Це означає дві речі: по-перше, потрібна жорстка клінічна валідація порогів; по-друге, лікарня мусить мати людей і час, щоб розгрібати цей новий потік роботи.
Скептики звертають увагу, що частина знайдених пухлин могла бути «очевидною» для добре натренованого рентгенолога. Звідси висновок: найсильніший ефект ШІ може бути там, де немає вузьких панкреатологів і бракує досвіду, — у районних лікарнях або центрах із малим обсягом складних випадків.
Паралельно існує стратегічна дилема: скринінг груп ризику проти масового пошуку. У багатьох країнах схиляються до моделі високого ризику, бо поширеність раку низька. Китай тестує іншу логіку — «піймай на шляху», використовуючи вже зроблені КТ як дешеву сировину для аналізу.
Регуляторна й комерційна траєкторія прискорюється. Повідомлялося, що FDA надала PANDA статус Breakthrough Device — пріоритетний супровід для технологій діагностики тяжких станів. Це не «дозвіл на продаж», а швидший коридор перевірок і комунікацій із регулятором.
 Відвідувачі лікарні Нінбо — Андреа Верделлі
Відвідувачі лікарні Нінбо — Андреа Верделлі
На землі технологія впирається в інфраструктуру. Лікарі в Нінбо визнають брак персоналу, щоб швидко контактувати з усіма пацієнтами, яких треба викликати. Додається й техніка: застаріле обладнання інколи не витримує обсягів даних, система підвисає, а це з’їдає час лікарів і довіру до інструмента.
Є й соціальний фактор, який часто недооцінюють у презентаціях A.I. У Китаї розмови про медичну корупцію підірвали довіру до лікарень, тому люди без симптомів можуть відмовлятися від повторного виклику, підозрюючи «втягування» у платні процедури. Для скринінгу довіра — така ж важлива, як і точність.
Тому майбутнє подібних систем — у протоколах і прозорості. Пацієнт має розуміти, що алгоритм лише підказує ризик, а рішення ухвалює лікар за стандартом. Потрібні чіткі маршрути: який тест далі, які терміни, які критерії зупинки, і як мінімізувати зайве опромінення та витрати для здорових людей.
Клінічна користь також залежить від того, що саме алгоритм підсвічує. PANDA може плутати пухлину з панкреатитом або не визначити, чи ураження первинне в підшлунковій, чи це метастаз. Тож навіть при сильному «пошуку» потрібні спеціалісти, здатні швидко поставити уточнювальні питання та відсікти шум.
Якщо подальші дані покажуть, що раннє виявлення реально зростає без лавини зайвих перевірок, Китай отримає робочий шаблон для онкологічної діагностики на рівні популяції. Якщо ні — алгоритм залишиться корисною підстраховкою для радіолога та інструментом навчання, але не «масовим сканером долі».
Для читача висновок прагматичний: ШІ в онкології — це не заміна лікаря, а система управління увагою. Вона може знайти те, що люди пропускають, але створює нові витрати, нові страхи і потребує ресурсів. У гонці за впровадженням переможе не найгучніший алгоритм, а найкраще організована медицина.




































